Artigo escrito por: Daniela Costa/ Revisado por: Paola Cappelletti
Olá, prezados leitores!
Na segunda edição da nossa newsletter, abordaremos o Teste de Ames, um procedimento essencial na avaliação da segurança de produtos químicos e compostos.
O Teste de Ames, nomeado em homenagem ao seu criador, o Dr. Bruce Ames, é uma técnica de triagem amplamente utilizada para avaliar a mutagenicidade de substâncias químicas. Este teste é baseado no uso de cepas bacterianas específicas, como Salmonella typhimurium e Escherichia coli, que foram geneticamente modificadas para não produzir um aminoácido essencial, como histidina (no caso de Salmonella) ou triptofano (no caso de E. coli). Essa modificação genética torna essas cepas bacterianas particularmente sensíveis a mutações.
Para ilustrar, tomemos o exemplo do sistema de teste que envolve Salmonella typhimurium incapaz de produzir histidina. A premissa fundamental desse teste reside na exposição dessas cepas mutantes a produtos químicos específicos (itens de teste que podem ser mutagênicos). Tendo a histidina como um aminoácido essencial para o crescimento celular, quando essas cepas são cultivadas em um meio que contém um item de teste mutagênico, o mesmo pode induzir uma mutação secundária no gene que codifica a histidina, substituindo a mutação original e promovendo a recuperação da capacidade dessa bactéria de sintetizar o aminoácido. Esse processo é conhecido como mutação reversa, e os produtos químicos que desencadeiam essa reversão são considerados mutagênicos.
Em termos práticos, nas culturas de S. typhimurium em que a reversão bacteriana não ocorre, não observamos a formação de muitas colônias. No entanto, nas cepas em que a reversão bacteriana acontece as colônias se desenvolvem em quantidade maior, isso indica que a substância testada causou uma segunda mutação, sendo, portanto, considerada mutagênica.
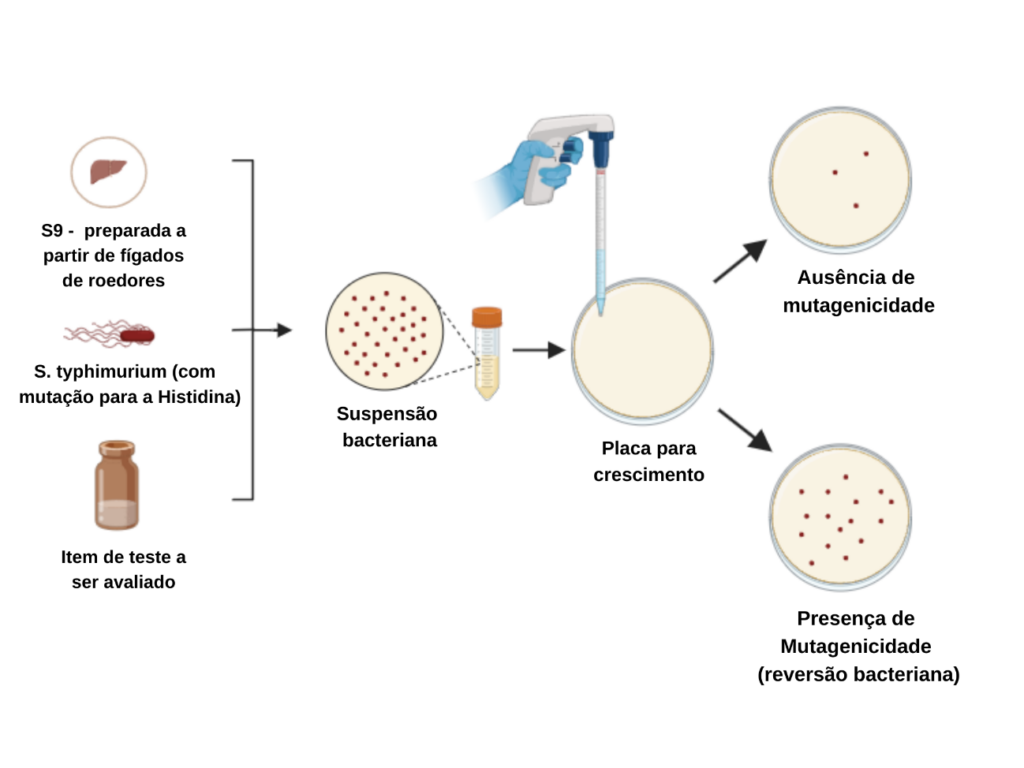
Realização do teste e suas diretrizes
Para garantir a validade dos resultados do Teste de Ames, é fundamental que as bactérias estejam na fase logarítmica do ciclo de crescimento, onde o número máximo de bactérias viáveis pode ser encontrado. Portanto, é crucial cultivar as bactérias até a fase exponencial tardia ou estacionária inicial, sendo desaconselhado o uso de culturas em fase estacionária tardia.
A seleção apropriada das cepas bacterianas é um passo crítico para o teste de Ames. Para obter resultados precisos e confiáveis, é necessário escolher cepas que sejam sensíveis a diferentes tipos de mutações. Além disso, seguir protocolos rigorosos é essencial para garantir a reprodutibilidade dos resultados. Um dos guias mais recomendados para a realização deste teste é o Guideline da OCDE TG nº 471, que estabelece diretrizes para o teste e é amplamente aceito internacionalmente. Esse documento está disponível gratuitamente no site da OCDE.
Normalmente, são usadas cinco cepas testadoras, dentre elas, quatro de Salmonella typhimurium (TA1535; TA1537 ou TA97a ou TA97; TA98; e TA100) e uma cepa E. coli WP2 uvrA, ou E. coli WP2 uvrA (pKM101), ou S. typhimurium TA102 em cada ensaio. O teste pode ser realizado por dois métodos convencionais: o Método de Incorporação de Placa Padrão e o Método de Pré-incubação. Em ambos os métodos, o item de teste é avaliado na presença e ausência de ativação metabólica (S9) para garantir a precisão dos resultados.
A incubação de todas as placas deve ser a 37°C durante 48-72 horas. Ao fim desse período, o número de colônias revertentes por placa é contabilizado. Um resultado positivo é caracterizado por um aumento dependente da concentração na frequência de reversão que excede os limites específicos da cepa. Para os resultados negativos, a interpretação é de que, nas condições do ensaio, o item de teste em estudo não é mutagênico nas espécies testadas.
Neste vídeo, https://vimeo.com/468729195, é possível conferir uma breve explicação sobre a realização do teste.
Momento apropriado para realizar o teste
Apesar de muitas empresas frequentemente não examinarem seus compostos quanto à mutagenicidade nas fases iniciais de desenvolvimento, essa não é uma prática recomendável, pois pode resultar em desperdício de tempo e recursos. Incorporar o teste de Ames nas fases iniciais do desenvolvimento de um produtos é crucial, especialmente quando é essencial avaliar a segurança de compostos. Isso permite a identificação precoce de potenciais problemas, economizando tempo e recursos a longo prazo.
O teste de Ames pode ser realizado em diversas situações, incluindo triagem de compostos, atendimento a requisitos REACH para o comércio na Europa, avaliação de impurezas, como nitrosaminas, e procedimentos de teste de Ames em conformidade com diretrizes específicas.
Em casos de recursos limitados, versões de triagem do teste de Ames podem ser utilizadas, como testes com ativação metabólica, doses máximas reduzidas, menos placas replicadas e redução do número de estirpes bacterianas examinadas. No entanto, é importante destacar que essas versões de triagem podem ter dificuldade em detectar mutagênicos fracos.
O impacto de um teste de Ames positivo
Um resultado positivo no teste de Ames indica que a substância testada tem o potencial de causar mutações genéticas, o que é uma preocupação significativa, uma vez que mutações podem levar ao desenvolvimento de câncer e outros problemas de saúde. Como resultado, um teste de Ames positivo pode desencadear investigações mais aprofundadas e, em alguns casos, pode resultar na interrupção do uso da substância ou do desenvolvimento de um produto. No entanto, é importante ressaltar que um teste positivo por si só não determina se uma substância é carcinogênica em seres humanos, mas serve como um indicador preocupante.
O Teste de Ames como alternativa ao uso de animais
Nos últimos anos, houve um movimento significativo para reduzir ou eliminar o uso de animais em pesquisas. Nesse contexto, o Teste de Ames se destaca como um método alternativo, uma vez que fornece uma maneira de avaliar a mutagenicidade in vitro, substituindo a necessidade de utilizar modelos animais para avaliação da mutagenicidade. Essa abordagem está alinhada com a crescente preocupação com o bem-estar animal e a busca por métodos mais éticos na pesquisa científica.
No Banco de Células do Rio de Janeiro estamos comprometidos em promover continuamente testes e ensaios que substituam, reduzam e refinem o uso de animais em experimentações. Como parte desse compromisso, temos o Teste de Ames disponível em nosso catálogo, proporcionando uma abordagem ética e eficaz na avaliação da segurança de produtos químicos. Continuaremos a inovar e avançar, buscando alternativas que priorizem o bem-estar animal e a excelência na pesquisa científica.
Referências:
Vijay U, Gupta S, Mathur P, Suravajhala P, Bhatnagar P. Microbial Mutagenicity Assay: Ames Test. Bio Protoc. 2018 Mar 20;8(6):e2763. https://doi.org/10.1016/B978-0-12-804667-8.00003-1. PMID: 34179285; PMCID: PMC8203972.
OECD (2020). Test No. 471: Bacterial Reverse Mutation Test. OECD Guidelines for the Testing of Chemicals, Section 4, OECD Publishing, Paris. Disponível em: https://doi.org/10.1787/9789264071247-en.
Jain, A.K., Singh, D., Dubey, K., Maurya, R., Mittal, S., Pandey, A.K. (2018). Models and Methods for In Vitro Toxicity. In: Dhawan, A., Kwon, S. (Eds.), In Vitro Toxicology. Academic Press. ISBN 9780128046678. Disponível em: https://doi.org/10.1016/B978-0-12-804667-8.00003-1





